LA chimie au lycée : pourquoi utilise-t-on un outil si compliqué ?
Depuis le temps que je donne des cours de soutien en chimie, il y a une question à laquelle je ne parviens pas à répondre : A quoi servent les tableaux d’avancement ?
Enfin, si… je sais qu’il sert principalement à déterminer, dans le cas d’une réaction totale, quel est le réactif limitant et lequel est en excès. Mais la question que je me pose est la suivante : Pourquoi demande-t-on aux élèves d’utiliser un outil aussi compliqué alors qu’un simple calcul de proportionnalité suffit à répondre à toutes les questions ?
Voici à quoi ressemble un tableau d’avancement :
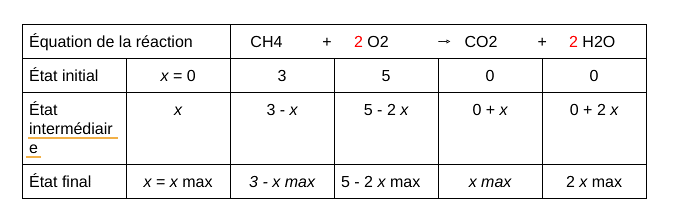
Le simple fait d’avoir à le tracer prend un temps fou qui distraie les élèves du problème posé. Ainsi, au lieu de se concentrer directement sur la réaction en elle-même, ils doivent sortir crayon et règle pour tracer ce tableau aussi complexe que difficile à comprendre. Ainsi, avant même de commencer à réfléchir, vous pouvez être sûr que nombre d’entre eux sont déjà en difficulté. Et outre cela, ce tableau mastodonte agit comme un voile sur la simplicité de ce qu’il y a à comprendre. Si vous ne savez pas comment ça marche, vous pouvez allez sur le site sherpas.com auquel j’ai emprunté l’image ci-dessus : vous jugerez par vous-mêmes…
Mais avant cela, je vous invite à lire les quelques lignes qui suivent.
Il suffit d’un simple calcul de proportionnalité pour déterminer le réactif limitant…
Considérons la combustion du méthane CH4 :
CH4 + 2 O2 –> CO2 + 2 H2O
et imaginons que l’on ait 3 moles de méthane CH4 et 5 moles de dioxygène O2 en début de réaction.
Quel sera alors le réactif limitant ? Quel sera celui en excès ?
Pour répondre à cette question, il suffit de considérer les coefficients stœchiométriques de la réaction et de faire un calcul de proportionnalité, avec un tableau.
Prenons le cas du méthane : les coefficients de la réactions nous indiquent que
1 mole de CH4 réagit avec 2 moles de O2
donc si l’on a 3 moles de CH4 au départ, il faudra deux fois de O2 pour que le méthane soit entièrement consommé, donc 6 moles. Or il n’y a que 5 moles de O2, donc il n’y a pas assez de dioxygène pour que tout le méthane soit consommé : le méthane est en excès et le dioxygène est en défaut. Et voilà, c’est (quasiment) fini !
Un autre exemple avec un tableau de proportionnalité cette fois.
Vous souhaitez savoir combien il restera de méthane à la fin de la réaction ? Alors prenons le problème dans l’autre sens, à partir du dioxygène.

On utilise la colonne jaune, ici, pour écrire les coefficients stœchiométriques de la réaction, puis on indique qu’on a 5 moles de dioxygène à notre disposition. On peut ainsi calculer combien de méthane sera nécessaire en faisant un produit en croix et on trouve : 5*1/2 = 2,5. On conclue que 2.5 moles de méthane seront consommées. Et on peut dire qu’il en restera 2 – 1.5 = 0.5 mole.
Vous aurez remarqué qu’en procédant ainsi on reste concentré sur l’essentiel, c’est-à-dire la réaction et les quantités mises en jeu : l’esprit n’est pas distrait par une procédure trop longue.
Pourquoi faire des tableaux d’avancement ?
Je reviens donc à ma question de départ. Pourquoi on fait des tableaux d’avancement si compliqués alors que de simples calculs de proportionnalité suffisent ?
Si vous avez une réponse, merci de me le faire savoir.

Pour toute commandes, rendez-vous sur la boutique de la mémogination.
